Premier principe thermodynamique : conservation de l'énergie
Energie totale
L'énergie totale d'un système isolé reste constante. Lavoisier : « Rien ne se perd, rien ne se crée, tout se transforme ».
Pour un système en mouvement (ΔEcinétique positive) et en interaction avec environnement extérieur (ΔEpotentielle non nulle),
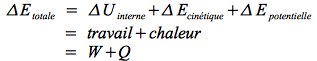
où U, fonction d'état extensive, représente l'énergie interne.
Pour un système au repos (ΔEcinétique = ΔEpotentielle = 0) et subissant une transformation thermodynamique (ex. changement d'état) d'un état d'équilibre A vers un état d'équilibre B :
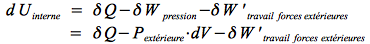
Remarque : Le premier principe considère toutes les transformations comme également possibles: il ne tient pas compte du caractère irréversible d'une transformation et ne se prononce pas sur la notion d'irréversibilité des transformations spontanées.
Définition d'un travail W
Travail = [ force de résistance Fi ] x [ déformation dXi de propriété extensive ].
convention le travail reçu par le système, dans ce cas dXi=Xfinal-Xinitial.
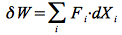
ex. déformation de volume = travail des forces de pression






