La liaison covalente
La figure ci-contre montre la forme de l'énergie potentielle en fonction de la distance entre les centres des noyaux de deux atomes d'hydrogène.
énergie totale est négative en chimie quantique → "énergie nulle" = tous les électrons et noyaux sont infiniment éloignés et donc sans interactions.
énergie minimale E° = système stable et correspond généralement à l'état fondamental.
La liaison ne se "décrète" pas : elle est un résultat.
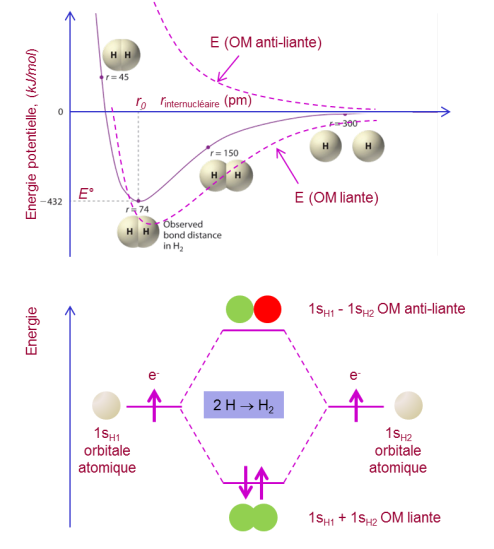
Molécule de H2 : Energie potentielle en fonction de la distance internucléaire et diagramme d'énergie des orbitales moléculaires
La liaison chimique covalente = présence d'un doublet d'électrons dans orbitale moléculaire liante de la molécule et absence d'électrons dans l'orbitale moléculaire anti-liante.





